Los tumores ‘estrangulan’ sus vasos sanguíneos para evitar que los fármacos lleguen a su destino
El aumento de la masa tumoral provoca presiones en el interior del tumor que pueden obstruir los vasos sanguíneos, cerrando así el paso a los fármacos anticancerígenos
MADRID Actualizado: GuardarLa angiogénesis es el proceso por el que se ‘crean’ nuevos vasos sanguíneos para proveer de oxígeno y nutrientes a los órganos y tejidos. Un proceso totalmente natural y necesario para el desarrollo embrionario y el crecimiento de cualquier organismo que, sin embargo, es también utilizado por los tumores para aumentar su volumen y colonizar nuevos órganos –la consabida ‘metástasis’–. Tal es así que, ya a día de hoy, los inhibidores de la angiogénesis –o ‘antiangiogénicos’– constituyen uno de los tipos de fármacos más utilizados para combatir el cáncer. Sin embargo, y en un gran número de ocasiones, ni los antiangiogénicos ni el resto de fármacos anticancerígenos son efectivos a la hora de detener el crecimiento tumoral. Y no porque no sean eficaces o los tumores desarrollen resistencia.
Lo que sucede, como muestra un estudio llevado a cabo por investigadores del Colegio Universitario de Londres (Reino Unido), es que el propio tumor ‘estrangula’ sus vasos sanguíneos durante su crecimiento y evita así, aun sin ninguna premeditación, que los fármacos alcancen su destino.
Como concluye Vasileios Vavourakis, director de esta investigación publicada en la revista « PLOS Computational Biology», «la vascularización juega un papel clave en el crecimiento, invasión y metástasis tumoral. Así, y con objeto de comprender los procesos biofísicos que tienen lugar durante este proceso y su importancia, es importante desarrollar modelos matemáticos fisiológicamente representativos y comparar sus resultados con los alcanzados en los datos experimentales. Distintos estudios han aplicado con éxito este enfoque para evaluar el efecto de diversos factores bioquímicos sobre el crecimiento tumoral y la angiogénesis. Sin embargo, estos modelos no han tenido en cuenta el efecto de las fuerzas mecánicas inducidas por el crecimiento sobre la evolución de la red angiogénica».
Vasos ‘comprimidos’
Numerosos estudios han demostrado que los tumores sólidos, caso entre otros muchos del glioblastoma multiforme o de los tumores de pulmón o de mama, emplean señales bioquímicas que promueven el crecimiento de nuevos vasos sanguíneos para obtener nutrientes que permitan su crecimiento y expansión por el organismo. Sin embargo, se desconoce cómo afectan las fuerzas mecánicas ejercidas por un tumor en crecimiento sobre estos nuevos vasos sanguíneos.
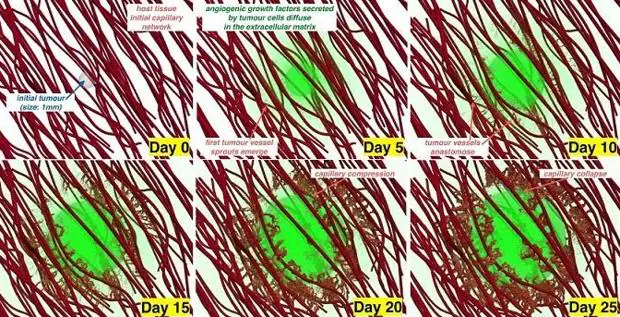
Por ello, los autores han desarrollado un modelo informático tridimensional para simular la angiogénesis durante la proliferación tumoral y analizar cómo las fuerzas mecánicas o ‘presiones’ que tienen lugar durante este crecimiento afectan a los vasos sanguíneos que se encuentran en el tumor.
El nuevo modelo demuestra que el tumor en crecimiento comprime y, en ocasiones, llega a ‘estrangular’ y ‘volatilizar’, sus propios vasos sanguíneos, impidiendo así la llegada del flujo sanguíneo a algunas partes del tumor. Un efecto que, entre otras consecuencias, puede imposibilitar la llegada de oxígeno al tumor, lo que puede dar lugar a que adquiera un carácter más invasivo. Pero aún hay más; dado que los vasos se encuentran obturados, los fármacos no pueden alcanzar el interior del tumor, reduciéndose así en gran medida la eficacia de los tratamientos.
Finalmente, los autores recurrieron al ‘mundo real’ para tratar de validar su modelo virtual. Y para ello, analizaron la formación de nuevos vasos sanguíneos que tiene lugar durante la proliferación del cáncer de mama en un modelo animal –ratones– y compararon sus observaciones con las halladas en su modelo informático. Los resultados mostraron que el modelo simulaba la angiogénesis tumoral de una forma más precisa cuando, además de los procesos bioquímicos que se utilizan en el resto de investigaciones, se tenían en cuenta las fuerzas mecánicas. Es decir, con objeto de lograr una mejor comprensión de lo que sucede en el interior de un cáncer, deben también tenerse en cuenta las presiones que se producen dentro del tumor durante su crecimiento.
Factores biofísicos
En definitiva, la eficacia o el fracaso de un tratamiento se encuentran condicionados, además de por múltiples factores biológicos –caso, por ejemplo, del desarrollo de resistencias por las células cancerígenas–, por aspectos meramente físicos, como son las tensiones y presiones que se producen en el interior del tumor por el aumento de su volumen.
Como concluye Vasileios Vavourakis, «nuestro siguiente paso será combinar nuestro modelo informático con investigaciones experimentales para mejorar la administración de los fármacos anticancerígenos y la eficacia de la radioterapia. Nuestro objetivo es reducir la dependencia actual de los estudios con modelos animales para el desarrollo de terapias frente al cáncer y diseñar ensayos clínicos con humanos más efectivos».
Ver los comentarios